Valami jó, számolni való hétköznapi téma?
1,129 views
Skip to first unread message
Attila Válinth
Oct 3, 2014, 6:52:28 AM10/3/14
to szamo...@googlegroups.com
Sziasztok!
Na? :)
Pipás
Oct 3, 2014, 8:38:49 AM10/3/14
to szamo...@googlegroups.com
Esetleg a víz forráspontja zárt térben a nyomás függvényében?
Attila Válinth
Oct 3, 2014, 10:19:41 AM10/3/14
to szamo...@googlegroups.com
Ha a nyomást növeljük a forráspont is növekszik...
Pipás
Oct 3, 2014, 11:09:12 AM10/3/14
to szamo...@googlegroups.com
Ez az. Milyen arányban? Hogy lehet kiszámolni? :)
ZilogR
Oct 3, 2014, 12:27:11 PM10/3/14
to szamo...@googlegroups.com
2014. október 3., péntek 12:52:28 UTC+2 időpontban Attila Válinth a következőt írta:
Sziasztok!Na? :)
Pipás
Oct 3, 2014, 12:41:37 PM10/3/14
to szamo...@googlegroups.com
:D
Attila Válinth
Oct 3, 2014, 2:37:14 PM10/3/14
to szamo...@googlegroups.com
:) Szigony utca?
ZilogR
Oct 4, 2014, 5:32:12 AM10/4/14
to szamo...@googlegroups.com
??? Laktunk arrafelé, de ezzel a csajjal nem találkoztunk... :-o Emlékeznék rá, asszem, ilyen sárga karórát nem lehet elfelejteni ;) :) :D
Számolni akarol? Engem most leginkább az érdekel, h a 2013-as észak koreai föld alatti nukleáris robbantás mekkora hatóerejű volt, azaz hány kilotonna TNT-nek felelt meg, amit ott elpukkantottak. Azon küzdök, hogy kapjak erre egy jó számot. :) Szálljatok be az agyalásba. :)
Számolni akarol? Engem most leginkább az érdekel, h a 2013-as észak koreai föld alatti nukleáris robbantás mekkora hatóerejű volt, azaz hány kilotonna TNT-nek felelt meg, amit ott elpukkantottak. Azon küzdök, hogy kapjak erre egy jó számot. :) Szálljatok be az agyalásba. :)
Pipás
Oct 4, 2014, 11:29:49 AM10/4/14
to szamo...@googlegroups.com
Becslések szerint 6-7 kt. De ezen már biztos túl vagy...
http://korkep.sk/cikkek/kulugyek/2013/02/17/13002
http://korkep.sk/cikkek/kulugyek/2013/02/17/13002
ZilogR
Oct 4, 2014, 3:55:58 PM10/4/14
to szamo...@googlegroups.com
Igazából én akarom a becslést megcsinálni. Egy jó módszer lenne rá: az ismert föld alatti nukleáris robbantások adataiból kell egy skálát csinálni (pl.: mekkora erősségű "földrengést" okoztak a Richter skálán) és ez alapján elhelyezni ezt. Érdekes módon, az összes ilyen adat elérhető a neten.
Vagy lehet olyan módszert keresni, mint az első atombomba robbantásnál volt: amikor megjelentek a képek róla, amin volt idő és távolságlépték, dimenzióanalízissel kerestek kapcsolatot a lökéshullám terjedése, a robbanás óta eltelt idő és a felszabadult energia között, amiből meg tudták becsülni, hány kilotonnás volt a bomba (ami akkoriban még titok volt). Persze itt időben nincs semmi ilyen adatunk, hacsak a távolság az epicentrumtól nem ad ilyen infót - de ehhez az egyes földrengés figyelő központok adatait kellene begyűjteni, ami szinte lehetetlen.
Persze megint én mondtam valamit, nem kell ám ebben követni. Nameg ez nem is hétköznapi. Valami sokkal klasszabb dolog kellene...
Vagy lehet olyan módszert keresni, mint az első atombomba robbantásnál volt: amikor megjelentek a képek róla, amin volt idő és távolságlépték, dimenzióanalízissel kerestek kapcsolatot a lökéshullám terjedése, a robbanás óta eltelt idő és a felszabadult energia között, amiből meg tudták becsülni, hány kilotonnás volt a bomba (ami akkoriban még titok volt). Persze itt időben nincs semmi ilyen adatunk, hacsak a távolság az epicentrumtól nem ad ilyen infót - de ehhez az egyes földrengés figyelő központok adatait kellene begyűjteni, ami szinte lehetetlen.
Persze megint én mondtam valamit, nem kell ám ebben követni. Nameg ez nem is hétköznapi. Valami sokkal klasszabb dolog kellene...
Message has been deleted
ZilogR
Oct 5, 2014, 2:28:24 PM10/5/14
to szamo...@googlegroups.com
Az előző törölt hozzászólásnál biztosan volt vmi jópofaság, kár, h törölve lett...
Ezek szerint nincs ötlet? Ha fizetnétek érte, ez egy piaci igény, amin lehetne keresni egy kis manit ;)
Ez olyan Szinbád problémája: hogyan fizessek a nekem felkínált ötletekért, ha nem tudom, milyen jó vagy rossz ötletek jönnek még a későbbiekben - de az éppen aktuális ötletelőt ki kell fizetnem. Ez nem is rossz, ezen van értelme agyalni.
Vagy: sokan lehúzzák vagy az egekbe magasztalnak egy-egy filmet. Hogyan lehet a valódi pontszámot megtudni, pl.: Port.hu-n vagy az IMDB-n?!?
Ezek szerint nincs ötlet? Ha fizetnétek érte, ez egy piaci igény, amin lehetne keresni egy kis manit ;)
Ez olyan Szinbád problémája: hogyan fizessek a nekem felkínált ötletekért, ha nem tudom, milyen jó vagy rossz ötletek jönnek még a későbbiekben - de az éppen aktuális ötletelőt ki kell fizetnem. Ez nem is rossz, ezen van értelme agyalni.
Vagy: sokan lehúzzák vagy az egekbe magasztalnak egy-egy filmet. Hogyan lehet a valódi pontszámot megtudni, pl.: Port.hu-n vagy az IMDB-n?!?
ZilogR
Oct 5, 2014, 2:40:06 PM10/5/14
to szamo...@googlegroups.com
Saját tudatlanságomnak tudható be, hogy nem Szinbád, hanem Szindbád és itt egy link hozzá: Válaszd a legjobbat!
Message has been deleted
ZilogR
Oct 6, 2014, 5:57:07 PM10/6/14
to szamo...@googlegroups.com
:-D minden jó benne, kivéve a legelső osztást, ami egy szorzás igazából. Azzal a moláris párolgáshő 40.6kJ/kg és ezt behelyettesítve megkapjuk a vélhetőleg helyes ~3500Pa/K értéket vagy ennek a reciprokát: 28.5K/bar értéket.
ZilogR
Oct 7, 2014, 3:32:30 AM10/7/14
to szamo...@googlegroups.com
A számítás, ha valakinek kellene - nameg az előzőt ezennel töröltem is!
Akkor, kérem a következő hétköznapi számolandót! :DDD
BTW: Ezzel a Clausius-Clapeyronnal meg lehet csinálni, h kiszámolja vki a fázisátmenet görbét a T-p diagramban, azzal meg lehet mindenféle levegő páratartalom dolgokat számolni meg mérni, meg stb...
Akkor, kérem a következő hétköznapi számolandót! :DDD
BTW: Ezzel a Clausius-Clapeyronnal meg lehet csinálni, h kiszámolja vki a fázisátmenet görbét a T-p diagramban, azzal meg lehet mindenféle levegő páratartalom dolgokat számolni meg mérni, meg stb...
ZilogR
Oct 7, 2014, 3:36:41 AM10/7/14
to szamo...@googlegroups.com
...időközben utána is néztem, az Atkins-ban (Atkins: Fizikai kémia I. kötet) is a vizet hozzák példának és kiszámolják ugyanezt a hármaspontra és a forráspontra, ott is 28K/bar, tehát helyben is vagyunk!
Pipás
Oct 7, 2014, 4:39:41 AM10/7/14
to szamo...@googlegroups.com
Ezt a témát ugye én vetettem fel.
Írtam már nektek is hogy előszedtem apám közel 20 éve porosodó gőzgépmodelleit és újra életet leheltem beléjük. Voltam már velük 2 bemutatón, összejöttem mostani (főleg hajós) gőzgépmodellezőkkel. Az ő fórumukon kérdezte valaki, miért tartják akkora mumusnak a gőzkazánt, mikor annál sokkal nagyobb nyomáson is baj nélkül üzemeltetnek nyomástartó edényeket. (Levegőtartály, tűzoltópalack, stb.)
Agyaltam a dolgon, és a következőkre jutottam:
A kazánban az előzőekkel ellentétben halmazállapotváltozás zajlik le. Vízből lesz gőz. Az állapotváltozás ideje alatt a hőmérséklet állandó nyomáson nem változik, a vízé megegyezik a gőzével. (Rejtett hő.)
Zárt térben azonban a gőzfejlődés miatt nő a nyomás. A nyomás növekedésével nő a forráspont. (Kukta.) Minden hőmérséklethez tartozik egy nyomásérték ahol a rendszer egyensúlyban van. Ilyenkor a gőz telített, nem képes több vízpárát befogadni. Ha most egy valamilyen kazánsérülés miatt a nyomás hirtelen leesik, a fenti hőmérséklet-nyomás egyensúly felborul és igyekszik helyreállni. Ez a bevitt energia (rejtett hő) miatt gőzirányba történik. A kialakult kisebb nyomáson immár túlhevítetté vált víz robbanásszerűen gőzzé alakul és ez okozza a kazánrobbanást. Persze a max. 2-2.5 atm nyomáson üzemelő modelleknél ez ritkán fordul elő...
Érdekelt még, hogy függ a hőmérséklet a nyomástól. Én is ráakadtam a Wikipédián a Clausius–Clapeyron-egyenletre.
http://hu.m.wikipedia.org/wiki/Clausius–Clapeyron-egyenlet
Én ebből a következőket tudtam leszűrni:
1. A hőmérséklet növelésével a nyomás exponenciálisan nő.
2. Az egyenletet a gyakorlati számításokhoz integrálni kell.
3. Az integráláshoz kell egy C állandó, amit gyakorlati méréssel lehet meghatározni. :(
Az 1. pontból következik amit már máshol is olvastam: Egyre kevesebb plusz hőközléssel érhetünk el egyre nagyobb nyomást. Vagyis nagyobb nyomáson a gőzgép gazdaságosabban üzemeltethető. Ez elméletileg 373 celsiusig igaz, ahol a víz szuperkritikus állapotba kerül. Itt a nyomás 217 bar.
http://hu.m.wikipedia.org/wiki/Hármaspont#A_szuperkritikus_v.C3.ADz
A 3. pontból meg az következik hogy tovább kutakodtam. Így akadtam rá egy jó közelítő értéket adó formulára, amivel egyszerűen kiszámolható az adott nyomáshoz tartozó hőmérséklet.
http://www.ajdesigner.com/phpvaporpressure/l_water_vapor_pressure_equation_temperature.png
Itt T a hőmérséklet Celsius fokban, P a nyomás hgmm-ben, A=8.14019, B=1810.94, C=244,485. Ezek az állandók a víz 99-374 fok Celsius közötti hőmérsékletén érvényesek.
Ezt a képletet egy kicsit átalakítottam. A P-t megszoroztam 760-al és hozzáadtam 1-et. Valamint A B C-t behelyettesítve:
T= 1810.94/(8.14019-log(760*(P+1)))-244.485
Így a feszmérő által mutatott nyomást lehet megadni atmoszférában, ami légköri nyomáson 0. Az így kiszámolt hőmérséklet értékek 0-2.5 atm között:
0-99.84 fok C, 0.5-111.77, 1-120.75, 1.5-128.03, 2-134.19, 2.5-139.57.
Ezeket az 50g-vel számoltam ki. Beírtam az egyenletet az Y szerkesztőbe, grafikusan ábrázoltam és megnéztem a hozzá tartozó táblázatot (Table) ahol tetszőleges tartomány és lépésköz állítható be.
Ha gondoljátok (Ext :) ) lehetne írni (esetleg) (közösen(!)) egy 15C programot a témában ami letárolja az állandókat, bekéri a nyomást és számol.
A fenti egyenletről és együtthatóiról itt is olvashattok.
http://en.m.wikipedia.org/wiki/Antoine_equation
Egyébként meg a fenti dolog főleg úgy jött össze hogy mostanában taxizgatok, tabletem van és nap közben van ifőm vele szarókázni. :)
Írtam már nektek is hogy előszedtem apám közel 20 éve porosodó gőzgépmodelleit és újra életet leheltem beléjük. Voltam már velük 2 bemutatón, összejöttem mostani (főleg hajós) gőzgépmodellezőkkel. Az ő fórumukon kérdezte valaki, miért tartják akkora mumusnak a gőzkazánt, mikor annál sokkal nagyobb nyomáson is baj nélkül üzemeltetnek nyomástartó edényeket. (Levegőtartály, tűzoltópalack, stb.)
Agyaltam a dolgon, és a következőkre jutottam:
A kazánban az előzőekkel ellentétben halmazállapotváltozás zajlik le. Vízből lesz gőz. Az állapotváltozás ideje alatt a hőmérséklet állandó nyomáson nem változik, a vízé megegyezik a gőzével. (Rejtett hő.)
Zárt térben azonban a gőzfejlődés miatt nő a nyomás. A nyomás növekedésével nő a forráspont. (Kukta.) Minden hőmérséklethez tartozik egy nyomásérték ahol a rendszer egyensúlyban van. Ilyenkor a gőz telített, nem képes több vízpárát befogadni. Ha most egy valamilyen kazánsérülés miatt a nyomás hirtelen leesik, a fenti hőmérséklet-nyomás egyensúly felborul és igyekszik helyreállni. Ez a bevitt energia (rejtett hő) miatt gőzirányba történik. A kialakult kisebb nyomáson immár túlhevítetté vált víz robbanásszerűen gőzzé alakul és ez okozza a kazánrobbanást. Persze a max. 2-2.5 atm nyomáson üzemelő modelleknél ez ritkán fordul elő...
Érdekelt még, hogy függ a hőmérséklet a nyomástól. Én is ráakadtam a Wikipédián a Clausius–Clapeyron-egyenletre.
http://hu.m.wikipedia.org/wiki/Clausius–Clapeyron-egyenlet
Én ebből a következőket tudtam leszűrni:
1. A hőmérséklet növelésével a nyomás exponenciálisan nő.
2. Az egyenletet a gyakorlati számításokhoz integrálni kell.
3. Az integráláshoz kell egy C állandó, amit gyakorlati méréssel lehet meghatározni. :(
Az 1. pontból következik amit már máshol is olvastam: Egyre kevesebb plusz hőközléssel érhetünk el egyre nagyobb nyomást. Vagyis nagyobb nyomáson a gőzgép gazdaságosabban üzemeltethető. Ez elméletileg 373 celsiusig igaz, ahol a víz szuperkritikus állapotba kerül. Itt a nyomás 217 bar.
http://hu.m.wikipedia.org/wiki/Hármaspont#A_szuperkritikus_v.C3.ADz
A 3. pontból meg az következik hogy tovább kutakodtam. Így akadtam rá egy jó közelítő értéket adó formulára, amivel egyszerűen kiszámolható az adott nyomáshoz tartozó hőmérséklet.
http://www.ajdesigner.com/phpvaporpressure/l_water_vapor_pressure_equation_temperature.png
Itt T a hőmérséklet Celsius fokban, P a nyomás hgmm-ben, A=8.14019, B=1810.94, C=244,485. Ezek az állandók a víz 99-374 fok Celsius közötti hőmérsékletén érvényesek.
Ezt a képletet egy kicsit átalakítottam. A P-t megszoroztam 760-al és hozzáadtam 1-et. Valamint A B C-t behelyettesítve:
T= 1810.94/(8.14019-log(760*(P+1)))-244.485
Így a feszmérő által mutatott nyomást lehet megadni atmoszférában, ami légköri nyomáson 0. Az így kiszámolt hőmérséklet értékek 0-2.5 atm között:
0-99.84 fok C, 0.5-111.77, 1-120.75, 1.5-128.03, 2-134.19, 2.5-139.57.
Ezeket az 50g-vel számoltam ki. Beírtam az egyenletet az Y szerkesztőbe, grafikusan ábrázoltam és megnéztem a hozzá tartozó táblázatot (Table) ahol tetszőleges tartomány és lépésköz állítható be.
Ha gondoljátok (Ext :) ) lehetne írni (esetleg) (közösen(!)) egy 15C programot a témában ami letárolja az állandókat, bekéri a nyomást és számol.
A fenti egyenletről és együtthatóiról itt is olvashattok.
http://en.m.wikipedia.org/wiki/Antoine_equation
Egyébként meg a fenti dolog főleg úgy jött össze hogy mostanában taxizgatok, tabletem van és nap közben van ifőm vele szarókázni. :)
Pipás
Oct 7, 2014, 4:42:32 AM10/7/14
to szamo...@googlegroups.com
Ifőm = időm. Ebből is látszik hogy tablet...
Pipás
Oct 7, 2014, 4:53:35 AM10/7/14
to szamo...@googlegroups.com
ZR, én a fenti témát pötyögtem, miközben összeadtunk. Most ügetek kajálni, de majd össze kéne hozni a 2 témát. Celsiusban. Vagyis 100 fok. 1 atm. 100 + hány fok C kell a 2 atm-hoz?
ZilogR
Oct 7, 2014, 6:14:23 AM10/7/14
to szamo...@googlegroups.com
Jó étvágyat!
Néhány pontba összeszedem:
a.) Antoine egyenletet is lehet használni, mint gáztörvényt, de első körben én az ideális gáztörvényt fogom használni (ahogyan azt is használtam a 2. pontban fent)
b.) 2bar-hoz 128.5C tartozna, de: ahogyan írod és ahogyan én is emlékszem, a T-p diagramban az állapot határ felfelé kunkorodó görbe, azaz kisebb hőfok fog kelleni, mint 128.5C. Ez csak a max. lehet!
c.) Tisztességtelen kicsit, de egy gőztáblázatot bárki megkukkanthat, ahonnan kiderül, hogy 120.2C lesz a jó - azaz helyes a megérzés, hogy 128.5C alatt lesz
d.) És igen, a Clausius-Clapeyron egyenlet csak egy érintőt ad, annak a meredekségét és bizony integrálni kell - de ezt is lehet könnyen csinálni, pl. egy sima Euler módszert ráengedve.
A d.) ponttal fogok jönni estefelé, ahogyan azt sejthetitek :))) - végre van egy kis élet ebben a csoportban!
Néhány pontba összeszedem:
a.) Antoine egyenletet is lehet használni, mint gáztörvényt, de első körben én az ideális gáztörvényt fogom használni (ahogyan azt is használtam a 2. pontban fent)
b.) 2bar-hoz 128.5C tartozna, de: ahogyan írod és ahogyan én is emlékszem, a T-p diagramban az állapot határ felfelé kunkorodó görbe, azaz kisebb hőfok fog kelleni, mint 128.5C. Ez csak a max. lehet!
c.) Tisztességtelen kicsit, de egy gőztáblázatot bárki megkukkanthat, ahonnan kiderül, hogy 120.2C lesz a jó - azaz helyes a megérzés, hogy 128.5C alatt lesz
d.) És igen, a Clausius-Clapeyron egyenlet csak egy érintőt ad, annak a meredekségét és bizony integrálni kell - de ezt is lehet könnyen csinálni, pl. egy sima Euler módszert ráengedve.
A d.) ponttal fogok jönni estefelé, ahogyan azt sejthetitek :))) - végre van egy kis élet ebben a csoportban!
ZilogR
Oct 7, 2014, 6:32:58 AM10/7/14
to szamo...@googlegroups.com
3. Az integráláshoz kell egy C állandó, amit gyakorlati méréssel lehet meghatározni. :(
Ejnye! Az integrálási állandót abból fogod tudni, hogy a görbének át kell mennie a t=100C, p=1atm ponton. Ha úgy nézem, valóban egy mérésből származó adatra van szükséged - és ez az: a víz normál légköri nyomáson 100C fokon forr. :)
Pipás
Oct 7, 2014, 10:50:38 AM10/7/14
to szamo...@googlegroups.com
Nosza rajta! Ez érdekesnek igérkezik... :)
ZilogR
Oct 7, 2014, 12:11:12 PM10/7/14
to szamo...@googlegroups.com
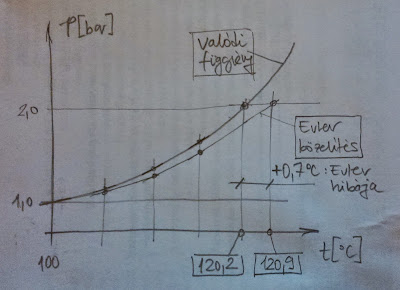
A kis CASIO fx-50F-em 140 másodperc futás után dT=0.1C lépésenkénti osztásban a fenti Clausius-Clapeyron egyenletet Euler módszerrel ledarálta és szerinte 2.001bar-hoz 120.9C tartozik az egyensúlyi görbén. :) Mivel az a görbe felfelé hajlik, ezért az érintők (Euler módszer) mindig alá lőnek a görbének, így nem is kell azon csodálkozni, hogy kicsit túlbecsüli a hőfokot (~0.7C-al). Annyit érdemes megjegyezni még, hogy bár kis mértékben, de a 2258kJ/kg párolgáshő is változik ám, ami szintúgy okoz egy kis eltérést!
Ezzel azt hiszem, elégedettek is lehetünk, ne várjunk egy ilyen "primitív" módszertől csodákat és ne is menjünk el a nagyobb pontosság (és hosszabb futásidők) irányába.
Már csak az a kérdés, h Pipás mit szeretne a továbbiakban?!? ;)
Ezzel azt hiszem, elégedettek is lehetünk, ne várjunk egy ilyen "primitív" módszertől csodákat és ne is menjünk el a nagyobb pontosság (és hosszabb futásidők) irányába.
Már csak az a kérdés, h Pipás mit szeretne a továbbiakban?!? ;)
Pipás
Oct 7, 2014, 2:01:47 PM10/7/14
to szamo...@googlegroups.com
Semmit, asszem már kellően kiveséztük. Még annyit hogy itt egy online kalkulátor, ez is az Antonie egyenletet használja.
http://www.ajdesigner.com/phpvaporpressure/water_vapor_pressure_equation_temperature.php#ajscroll
Eszerint:
2 bar: 120.325033852 celsius
2 atm: 120.74563326054 celsius
Abból is adódhat az eltérés h. 1 atm = 760 hgmm = 1,01325 bar.
http://www.ajdesigner.com/phpvaporpressure/water_vapor_pressure_equation_temperature.php#ajscroll
Eszerint:
2 bar: 120.325033852 celsius
2 atm: 120.74563326054 celsius
Abból is adódhat az eltérés h. 1 atm = 760 hgmm = 1,01325 bar.
Pipás
Oct 7, 2014, 2:19:21 PM10/7/14
to szamo...@googlegroups.com
Vagyis mivel az Antonie egyenlet közelítő értéket ad és a 120,2 höz képest .12-t tévedett, az eredményed akár lehet pontos is ha esetleg atm a mértékegysége.
ZilogR
Oct 7, 2014, 4:23:01 PM10/7/14
to szamo...@googlegroups.com
Én kezdőértéknek a 100000Pa-t és a 373.2K-t választottam. Nehezen visz rá a lélek, hogy 373.15-nek írjam, aminek az az oka valszeg, hogy az már túl sok értékes jegy :) (A brit területeken elterjedt 9.81 helyett használt 9.8-at viszont kevésnek érzem, bár néha-néha én is használom, ha lehet vele egy lépést spórolni vagy egy kis időt nyerni.)
Végértékként pedig a 2bar-t, azaz a 200000Pa-t.
Ez ellen nincs mit tenni, ha olyan a függvény, hogy alulról domború, akkor az Euler mindig laposabban fogja követni. Ez az oka, hogy túlbecsüli a hőfokot.
Megpróbálok egy prediktor-korrektor módszert beszorítani a kis CASIO 29 programlépésébe és az majd jobban "másolja" a függvény ívét.
Végértékként pedig a 2bar-t, azaz a 200000Pa-t.
Ez ellen nincs mit tenni, ha olyan a függvény, hogy alulról domború, akkor az Euler mindig laposabban fogja követni. Ez az oka, hogy túlbecsüli a hőfokot.
Megpróbálok egy prediktor-korrektor módszert beszorítani a kis CASIO 29 programlépésébe és az majd jobban "másolja" a függvény ívét.
ZilogR
Oct 7, 2014, 4:39:58 PM10/7/14
to szamo...@googlegroups.com
A lenti (fenti) rajzon látható, hogy miért becsül túl az Euler ebben az esetben. A mindig laposabban futó közelített függvénygörbe magasabb hőfoknál éri el a 2bar nyomásértéket.
Igazából a megírt kis Euler módszer által visszaadott hőmérséklet értékből le kellene vonnom a lépésköz felét, ezzel egy pontosabb közelítő értéket kapok: Az azt megelőző t-érték még nem volt jó, az aktuális pedig már túlment a 2bar-on, azaz a 0.1C-os osztás esetén amit én kaptam, az: (120.85 +/- 0.05)C
Igazából a megírt kis Euler módszer által visszaadott hőmérséklet értékből le kellene vonnom a lépésköz felét, ezzel egy pontosabb közelítő értéket kapok: Az azt megelőző t-érték még nem volt jó, az aktuális pedig már túlment a 2bar-on, azaz a 0.1C-os osztás esetén amit én kaptam, az: (120.85 +/- 0.05)C
ZilogR
Oct 8, 2014, 11:17:51 AM10/8/14
to szamo...@googlegroups.com
Na, és ki veszi rajta észre a hibát?!? ;) (nem nagy, de mégiscsak az)
ZilogR
Oct 8, 2014, 12:45:17 PM10/8/14
to szamo...@googlegroups.com
...és mivel élek-halok az efféle társalgásokért, kérem a következő morzsát elhinteni (Ext, pls!), hogy 2-3 napra meglegyen a "lúd" adagom ("Hozd a lúdot!") :D
http://youtu.be/6oHSd9tNLEc?t=2m28s
http://youtu.be/6oHSd9tNLEc?t=2m28s
Attila Válinth
Oct 12, 2014, 1:57:40 AM10/12/14
to szamo...@googlegroups.com
Egy régebbi felvetés:
"Ha már senki nem akar írni, akkor csináljatok egy olyat, ahol a SOLVE-t és az integrál-t együtt kell használni, pl. olyan integrál, amiben van egy ismeretlen paraméter vagy hogy még szebb legyen, az integrálási határ az ismeretlen." :)
ZilogR
Oct 12, 2014, 5:55:22 AM10/12/14
to szamo...@googlegroups.com
Akkor az elsőre egy feladat - Oroszországból szeretettel:
Mekkora legyen "a" értéke, hogy "f(x)" sűrűségfüggvény legyen? Ez egy integrál+solve együtt. Jó szórakozást :) Először papíron tessék megcsinálni, aztán a 15C-vel!
Mekkora legyen "a" értéke, hogy "f(x)" sűrűségfüggvény legyen? Ez egy integrál+solve együtt. Jó szórakozást :) Először papíron tessék megcsinálni, aztán a 15C-vel!
ZilogR
Oct 12, 2014, 6:20:45 AM10/12/14
to szamo...@googlegroups.com
Na, még nincs kész?!??!
:)
:)
Attila Válinth
Oct 12, 2014, 7:04:20 AM10/12/14
to szamo...@googlegroups.com
:/
Még át is kell nézni az alapokat...(is) :)
ZilogR
Oct 12, 2014, 7:14:14 AM10/12/14
to szamo...@googlegroups.com
- A sűrűségfüggvény olyan függvény, ami alatt a terület egyenlő 1-el.
- Tehát neked fel kell írnod a sűrűségfgv-t azon a szakaszon, ahol nem nulla, azaz a 0...3 intervallumon.
- Ha megvan f(x), akkor számold ki az integrált ezen a szakaszon, eredményképpen kapsz egy függvényt, amiben csak az "a" az ismeretlen.
- Ezt az eredményként kapott fgv-t kell egyenlővé tenned 1-el és abból kiszámolni "a"-t.
- Utána le is ellenőrizheted, h nem toltad-e el, pl.: megcsinálod az integrálást újra, már ismerve az "a"-t
- Aztán előkapod a 15C-t és arra kiagyalod, h hogyan lehet egy integrálás közben solverezni és azzal megcsinálod a feladatot megint.
ZilogR
Oct 12, 2014, 8:21:22 AM10/12/14
to szamo...@googlegroups.com
- Ha megvan f(x), akkor számold ki az integrált ezen a szakaszon, eredményképpen kapsz egy függvényt, amiben csak az "a" az ismeretlen.
- Ezt az eredményként kapott fgv-t kell egyenlővé tenned 1-el és abból kiszámolni "a"-t.
Igazából mindenki érti, h ez amolyan ágyúval verébre, mivel ez egy trapéz, de lehetne ez sokkal bonyolultabb is és akkor is működő módszert kell találni!
Attila Válinth
Oct 12, 2014, 2:59:48 PM10/12/14
to szamo...@googlegroups.com
Bakker ZilogR, de régen csináltam. Líneáris Fv. viszonylag egyszerű lenne. Deriválnom kellene, akkor megkapnám a meredekségét...:)
segíthetnél mán egy picit... De régen csináltam...
Na meg dolgozom is közben. ez a maszek világ :D
ZilogR
Oct 12, 2014, 5:18:28 PM10/12/14
to szamo...@googlegroups.com
ZilogR
Oct 12, 2014, 5:35:58 PM10/12/14
to szamo...@googlegroups.com
Vagy ha "felismerjük", hogy trapéz, akkor: (a+2×a)÷2×3=1 egyenletet kell megoldani a-ra, ami elvégezve a baloldali műveleteket: (9÷2)×a=1 --> a=2÷9 =~0.222
ZilogR
Oct 13, 2014, 4:46:22 PM10/13/14
to szamo...@googlegroups.com
A Clausius-Clapeyron egyenlettel 100'000Pa-hoz 373.2K-t "párosítva" a 200'000Pa-hoz pontosan 120.85C tartozik, azaz a sima Euler is egész jó eredményt ad.dT=0.1C osztásnál szinte tökéletes az eredmény, ahogy fentebb írtam is.
De ha dT=1C-al futtatom, akkor 205'300Pa végeredményt kapunk, amihez a 121.5C fog tartozni. Ezt csak amiatt írom le, hogy egy prediktor-korrektor módszer ugyanígy dT=1C osztással már 200'910Pa-t ad és ahhoz a 120.5C-t számítja. Ebből is látszik, hogy néha érdemes még a pontatlan felbontás mellett is pontosabb módszert választani, mert a futásidő nem nő meg jelentősen, de a kapott eredmény kárpótol.
De ha dT=1C-al futtatom, akkor 205'300Pa végeredményt kapunk, amihez a 121.5C fog tartozni. Ezt csak amiatt írom le, hogy egy prediktor-korrektor módszer ugyanígy dT=1C osztással már 200'910Pa-t ad és ahhoz a 120.5C-t számítja. Ebből is látszik, hogy néha érdemes még a pontatlan felbontás mellett is pontosabb módszert választani, mert a futásidő nem nő meg jelentősen, de a kapott eredmény kárpótol.
Message has been deleted
ZilogR
Oct 13, 2014, 5:04:03 PM10/13/14
to szamo...@googlegroups.com
A LBL4 fogja csinálni az integrálást, azt kell majd SOLVE-rezni és a LBL5 lesz maga a függvény, R0-ban lesz tárolva "a" értéke:
LBL 4 'A függvény, amit meg kell oldani a SOLVE-rrel
STO 0 'A SOLVE visszaadja a stack-be az ismeretlen éppen aktuális értékét, azt eltesszük "a"-ba
0 'Integrálási határok 0-tól
ENTER '...
3 '3-ig
∫ 5 'LBL 5 az f(x)
1 'A kapott integrálból levonjuk a várt görbe alatti területet, a SOLVE ezt az eltérést kapja
-
RTN
LBL 5 'f(x) számítása
3
+
3
÷
RCL×0 'itt szorzunk "a"-val ("a"-t R0-ban tároljuk)
RTN
A fenti kis programok használata egyszerű: 0 ENTER 1 f SOLVE 4.
84 másodperc futás után a kijelzőn megjelenik a 0.222 eredmény.
LBL 4 'A függvény, amit meg kell oldani a SOLVE-rrel
STO 0 'A SOLVE visszaadja a stack-be az ismeretlen éppen aktuális értékét, azt eltesszük "a"-ba
0 'Integrálási határok 0-tól
ENTER '...
3 '3-ig
∫ 5 'LBL 5 az f(x)
1 'A kapott integrálból levonjuk a várt görbe alatti területet, a SOLVE ezt az eltérést kapja
-
RTN
LBL 5 'f(x) számítása
3
+
3
÷
RCL×0 'itt szorzunk "a"-val ("a"-t R0-ban tároljuk)
RTN
A fenti kis programok használata egyszerű: 0 ENTER 1 f SOLVE 4.
84 másodperc futás után a kijelzőn megjelenik a 0.222 eredmény.
ZilogR
Oct 14, 2014, 5:33:03 AM10/14/14
to szamo...@googlegroups.com
Na, necsinájjátok eszt!
Amúgy tudom, h mi a gond, azt várja az ember, hogy valami ötvensoros programok lesznek itt, közben meg pár utasítás és megcsinálja.
Az ilyet sokkal nehezebb értelmezni, mint valami hosszú, nyögvenyelős, szájbarágós ömlengést...
Próbáljátok ki, már csak azért is, mert a svájci 15C-ben azért van kraft és érdekel mennyi ideig tart neki kiköpni az eredményt.
Amúgy tudom, h mi a gond, azt várja az ember, hogy valami ötvensoros programok lesznek itt, közben meg pár utasítás és megcsinálja.
Az ilyet sokkal nehezebb értelmezni, mint valami hosszú, nyögvenyelős, szájbarágós ömlengést...
Próbáljátok ki, már csak azért is, mert a svájci 15C-ben azért van kraft és érdekel mennyi ideig tart neki kiköpni az eredményt.
Attila Válinth
Oct 14, 2014, 8:35:46 AM10/14/14
to szamo...@googlegroups.com
Swiss: 4 sec...
ZilogR
Oct 14, 2014, 10:08:03 AM10/14/14
to szamo...@googlegroups.com
Wow, ez akkor 20x gyorsabb... Megérné a kis 15C-t újra kiadnia a HP-nek 64k RAM-mal és 100MHz környéki procival és USB csatlakozóval, de a régi fazonban (és Attila kedvéért egy "Mini" változatban is, de HP billentyűzettel :) ). Ehhez kellene már egy PC-s környezet is, ki akar keycode-okat bámulva programozni ;)
Akkor ha ez a feladvány is lement, jöhet a következő napi számolni való! De gyorsan ám, mert telhetetlen valék!
Akkor ha ez a feladvány is lement, jöhet a következő napi számolni való! De gyorsan ám, mert telhetetlen valék!
Attila Válinth
Oct 15, 2014, 7:12:46 AM10/15/14
to szamo...@googlegroups.com
Nem is olyan rossz kis masina ez.
Talán még kárpótol is a gyorsasága, strapabírása, kicsi energia fogyasztása a fránya "gombropogásokért" :)
Mi legyen a számolási téma?
neked mindig van ötleted...:)
ZilogR
Oct 15, 2014, 7:24:35 AM10/15/14
to szamo...@googlegroups.com
Épp az a gondom, h a szakmámból eredően én problémákat tudok megoldani - nem generálni! Az a Duna túlpartján levő egyetem! :D ;)
Mivel pedagógiai vénám is van, érdekel, h a két nyúlfarknyi programocskának minden porcikáját érted-e?!?
Mivel pedagógiai vénám is van, érdekel, h a két nyúlfarknyi programocskának minden porcikáját érted-e?!?
Attila Válinth
Oct 15, 2014, 7:45:23 AM10/15/14
to szamo...@googlegroups.com
Semmitsem:)
ZilogR
Oct 15, 2014, 7:49:31 AM10/15/14
to szamo...@googlegroups.com
Akkor ezzel beincepcionáltad az agyamba, hogy ezt oldjam meg, mint problémát!
Nem élhetsz úgy, hogy nem érted, mikor mi kerül a stack-be és mi kell a SOLVE ill. Integrál rutinnak, amikor meghívjuk, nameg mit csinálnak egymással, amikor egymást hívják...
Nem élhetsz úgy, hogy nem érted, mikor mi kerül a stack-be és mi kell a SOLVE ill. Integrál rutinnak, amikor meghívjuk, nameg mit csinálnak egymással, amikor egymást hívják...
Attila Válinth
Oct 15, 2014, 7:53:16 AM10/15/14
to szamo...@googlegroups.com
kommunikáció
Attila Válinth
Oct 15, 2014, 9:07:01 AM10/15/14
to szamo...@googlegroups.com
Na átnyálazom 2 meló közben.
Amúgy sajnos a HP32 SII nem kapcsol be...:(
ZilogR
Oct 15, 2014, 9:27:24 AM10/15/14
to szamo...@googlegroups.com
1.) Nyálazd! :)
2.) Akkor ebből hátlapletépős nagyjavítás lesz... :(
2.) Akkor ebből hátlapletépős nagyjavítás lesz... :(
Attila Válinth
Oct 17, 2014, 12:56:06 AM10/17/14
to szamo...@googlegroups.com
Sajnos
ZilogR
Oct 22, 2014, 12:42:42 PM10/22/14
to szamo...@googlegroups.com
Bízva abban, h a mostani "hosszú hétvége" alatt csak lesz egy kis számológépezés, csak lesz vkinek vmi jó ötlete...!!?!?
Attila: te olyanféle vagy, aki szeret furkálni és biztosan érdekel a geológia is.
Engem régóta érdekel a dinnyekopogtatás és hogy hogyan lehet ott bármit hallani. Nameg ez elvezet engem a föld alatti nukleáris kísérletekhez is, de az már más tészta, tehát, segíts nekem (nekünk):
Attila: te olyanféle vagy, aki szeret furkálni és biztosan érdekel a geológia is.
Engem régóta érdekel a dinnyekopogtatás és hogy hogyan lehet ott bármit hallani. Nameg ez elvezet engem a föld alatti nukleáris kísérletekhez is, de az már más tészta, tehát, segíts nekem (nekünk):
- Hogyan kell értelmezni a Richter-skálán megadott értékeket? Én elolvastam a wiki cikket, de vannak benne hiányos részek. Kellene egy rövid magyarázat, hogy hogyan is kell ezt a magnitudó dolgot érteni (akár könyvet is ajánlhatsz)
- Hogyan kell a Föld sajátfrekvenciáját meghatározni? Ez már elvezet a dinnyekopogtatás irányába, mert azzal hozható kapcsolatba, milyen hangot hallunk.
Plissz ikszplén dö öbov topix! :)
ZilogR
Oct 26, 2014, 11:16:44 AM10/26/14
to szamo...@googlegroups.com
- Newton-módszer lerágott csont, de tessék kicsit még nyalogatni:
1a.) Megoldandó az x^4-1=0 egyenlet a komplex számsíkon.
Erre kell írni egy Newton-módszeres megoldót, amit valamilyen kezdőértékről el kell startoltatni és megnézni, hogy a négy gyök ( 1+0i, -1+0i, 0+i és 0-i ) melyikéhez fog konvergálni?! Javasolt géptípus természetesen a 15C, de lehet más masinákon is dolgozni.
1b.) Ezután az a feladat, hogy egy négyzetrácsos papíron be kell színezni, a kezdőértéknek megfelelő pontot mondjuk kékre, zöldre, sárgára és pirosra annak megfelelően, hogy 1+0i, -1+0i, 0+i és 0-i gyökhöz konvergált-e a megoldó. Vajon mit lehet észrevenni? Egy tipp: ha az egyes iterációs lépések közbenső értékeit is kiíratjátok, akkor már azokat a pontokat is be lehet színezni, nem csak a kezdőpontot. Ezzel lehet egy kis időt nyerni. Tipp2: Érdemes egy durva ráccsal indulni és ha érdekes részt talál valaki, akkor finomítani. Amúgy ez egy igazi sziszifuszi munka, ezért jöjjön egy sokkal könnyebb: - (az első) Feigenbaum-állandó kiszámítása numerikusan
2a.) Egy rövidke VisualBASIC programmal lehet ilyesmiket rajzolni (Bifurkáció - Logisztikus leképezés), a hozzá kapcsolódó egyenleteket meg lehet találni a Wikipedia linken: Logistic map
2b.) A Feigenbaum-állandó egy arány, ami kapcsolatba hozható azokkal az egymás utáni értékekkel, ahol ez a bifurkációs diagram kettéágazik. Nyomozzátok ki, hogy mi is ez pontosan és mennyi lehet az értéke? Ne tessék nagyon komoly gépkapacitást igénybe venni, ugyanis Feigenbaum egy HP-65-össel oldotta meg ezt a problémát - azaz játszik minden programozható számológép, igen, én egy 12C-vel fogok versenybe szállni.
2014. október 3., péntek 12:52:28 UTC+2 időpontban Attila Válinth a következőt írta:
Sziasztok!Na? :)
ZilogR
Oct 27, 2014, 12:49:05 PM10/27/14
to szamo...@googlegroups.com
Na, akkor ti mondjatok - de Halloween-es legyen ám!
ZilogR
Oct 29, 2014, 11:33:43 AM10/29/14
to szamo...@googlegroups.com
Nekem még mindig tetszik ez a Clausius-Clapeyron, van vkinek kedve az iránymezőt kézzel felvázolni és belerajzolni az Euler-t?!? Tanulságos lenne, jól mutatná a lényeget...
ZilogR
Nov 7, 2014, 5:57:28 AM11/7/14
to szamo...@googlegroups.com
Na, Tolosa bement a csőbe, azt írta egy másik topikban, hogy kedveli a matematikai statisztikát.
Akkor egy hétköznapi és statisztika feladvány neki - és mindenki másnak:
Sajnos itthon kell töltenem pár napot és éppen a legújabb "Mániát" ragasztgatjuk: Van egy gyűjtőalbum, amiben 200db matricát kell gyűjteni.
Nekünk eddig éppen 80db van meg, azaz 120 hiányzik.
Tegnap kaptunk 185db matricát.
A kérdés: ha befejezzük a ragasztgatást, várhatóan hány matrica fog hiányozni?
a.) Kérem a tippeket és a tudományos értekezéseket és utána postolom az eredményt.
b.) A második körben az lesz persze a kérdés, vajon lehet-e mondani valamit arról a valószínűségről, hogy az eltérésünk az elméleti értéktől mennyire elfogadható, azaz cinkeltek-e a matricacsomagok?!?
Akkor egy hétköznapi és statisztika feladvány neki - és mindenki másnak:
Sajnos itthon kell töltenem pár napot és éppen a legújabb "Mániát" ragasztgatjuk: Van egy gyűjtőalbum, amiben 200db matricát kell gyűjteni.
Nekünk eddig éppen 80db van meg, azaz 120 hiányzik.
Tegnap kaptunk 185db matricát.
A kérdés: ha befejezzük a ragasztgatást, várhatóan hány matrica fog hiányozni?
a.) Kérem a tippeket és a tudományos értekezéseket és utána postolom az eredményt.
b.) A második körben az lesz persze a kérdés, vajon lehet-e mondani valamit arról a valószínűségről, hogy az eltérésünk az elméleti értéktől mennyire elfogadható, azaz cinkeltek-e a matricacsomagok?!?
Tolosa
Nov 7, 2014, 6:42:23 AM11/7/14
to szamo...@googlegroups.com
Azt nem írtam, hogy produkálni és vizsgáztatni is akarom magam, csak annyit, hogy kedvelem a matematikai statisztikát. Ez olyan 'magánvaló'-dolog.
A feladatod ebben a formában inkább hajazik egy valószínűségszámítási problémára, de -mivel semmit nem tudok a 'Mánia' nevű akármiről, így számomra hiányosnak tűnnek az alapadatok ahhoz, hogy ráhúzhassak valamilyen eloszlási formulát. /pl. milyen feltételnek kell megfeleljen a kiválasztandó matrica?/
Persze, ha beugratós a kérdés, akkor passz.
A feladatod ebben a formában inkább hajazik egy valószínűségszámítási problémára, de -mivel semmit nem tudok a 'Mánia' nevű akármiről, így számomra hiányosnak tűnnek az alapadatok ahhoz, hogy ráhúzhassak valamilyen eloszlási formulát. /pl. milyen feltételnek kell megfeleljen a kiválasztandó matrica?/
Persze, ha beugratós a kérdés, akkor passz.
ZilogR
Nov 7, 2014, 7:29:26 AM11/7/14
to szamo...@googlegroups.com
Ez a SPAR Szigetmánia (nem kapok egy fillért se ezért, se matricát :P )
Talán(?) lehet mondani, hogy egyenletes eloszlásban fordul elő a 200 féle matrica. Most van 120 üres helyünk, oda kell a 185db kapott matricát elkezdeni ragasztgatni. A kérdés az, ha a 185db-on végig megyek és amit tudok, beragasztom, mennyi fog még hiányozni a kiindulási 120db-ból?
Lehetne akár úgy is gondolkodni, hogy ha egyenletes eloszlásúak a matricák, akkor a 200db-ból nekem 120db a jó (mert az a jó, ha kapok a hiányzó helyre matricát) és ez a 185db között is ugyanúgy oszlik meg (mert egyenletes eloszlás), azaz 120÷200×185=111 matrica lesz jó és ekkor csak 9db fog hiányozni. Ez akár jó gondolat is lehetne, ha pl.: nem lennének egyformák a 185 között, így várhatóan a 9db helyett több fog a ragacsolás után hiányozni (elárulom, sokkal több hiányzik, talán nem is titok, hiszen mi mást is kaphattunk volna, mint a választ az életet, a világmindenséget, meg mindent érintő végső kérdésre :) :D ). Persze ez egy "kísérlet" eredménye, engem az érdekel, mennyi lenne ez elméletileg.
Ha erre megadjátok a választ (én is gondolkodom rajta, mert nincs időnk hét és fél millió évig várnunk), akkor az érdekel, hogy mennyire cinkelt az eredmény, azaz ez az eltérés eltérés-e vagy sem?!?
Talán(?) lehet mondani, hogy egyenletes eloszlásban fordul elő a 200 féle matrica. Most van 120 üres helyünk, oda kell a 185db kapott matricát elkezdeni ragasztgatni. A kérdés az, ha a 185db-on végig megyek és amit tudok, beragasztom, mennyi fog még hiányozni a kiindulási 120db-ból?
Lehetne akár úgy is gondolkodni, hogy ha egyenletes eloszlásúak a matricák, akkor a 200db-ból nekem 120db a jó (mert az a jó, ha kapok a hiányzó helyre matricát) és ez a 185db között is ugyanúgy oszlik meg (mert egyenletes eloszlás), azaz 120÷200×185=111 matrica lesz jó és ekkor csak 9db fog hiányozni. Ez akár jó gondolat is lehetne, ha pl.: nem lennének egyformák a 185 között, így várhatóan a 9db helyett több fog a ragacsolás után hiányozni (elárulom, sokkal több hiányzik, talán nem is titok, hiszen mi mást is kaphattunk volna, mint a választ az életet, a világmindenséget, meg mindent érintő végső kérdésre :) :D ). Persze ez egy "kísérlet" eredménye, engem az érdekel, mennyi lenne ez elméletileg.
Ha erre megadjátok a választ (én is gondolkodom rajta, mert nincs időnk hét és fél millió évig várnunk), akkor az érdekel, hogy mennyire cinkelt az eredmény, azaz ez az eltérés eltérés-e vagy sem?!?
Tolosa
Nov 7, 2014, 10:20:15 AM11/7/14
to szamo...@googlegroups.com
Nos, látod, erről beszéltem. Mert van a problémában néhány paraméter, ami számodra evidens, mert TUDOD, miről van szó. Máris közöltél egy kiegészítő információt, hogy -valószínűleg- az eloszlás típusa normál eloszlás. Ez közelebb vihet a probléma megfogalmazásához ugyan, de számomra még mindig nem elég világos maga a probléma. Az evidencia hiánya miatt /fogalmam nincs, mi a lótúró ez az egész Mánia-dolog és mi a lényege/ még mindig nem tudom, melyek a feltételek. Egyáltalán mely matricák ragaszthatók bele a készletbe? Mindegyik? Bármelyik, vagy csak bizonyos feltételeknek megfelelők?
Magyarul- már meg ne sértődj- 'Mánia' szempontból laikus számára pongyolán van megfogalmazva maga a probléma.
Vagy én vagyok nehézfejű. Hogy stílusos legyek, ennek sem nulla a valószínűsége.
Magyarul- már meg ne sértődj- 'Mánia' szempontból laikus számára pongyolán van megfogalmazva maga a probléma.
Vagy én vagyok nehézfejű. Hogy stílusos legyek, ennek sem nulla a valószínűsége.
Tolosa
Nov 7, 2014, 10:30:45 AM11/7/14
to szamo...@googlegroups.com
Egyébként ha úgy lenne megfogalmazva a feladat, hogy a feltételeknek megfelelő matricák számának eloszlása a teljes darabszámon belül normál eloszlást követ ÉS a neked rendelkezésre álló X db között 80 db volt a megfelelő, akkor számítható lenne, hogy az újabb 185 db közül Y megfelelő db előfordulásának mekkora a valószínűsége.
2014. november 7., péntek 11:57:28 UTC+1 időpontban ZilogR a következőt írta:
ZilogR
Nov 7, 2014, 11:17:53 AM11/7/14
to szamo...@googlegroups.com
Egyenletes eloszlású, azaz minden matrica egy végtelen nagy sokaságból ugyanakkora 1÷200 valószínűséggel választódik ki, NEM normális eloszlású!!!
Mi megcsináltuk a ragasztást és megszámoltuk az üresen maradt helyeket és azt kaptuk, hogy negyvenkettő.
Kérdés 1: mennyi lenne ez a 42 elméletileg, amit a fentiek ismeretében várhattunk volna?
Kérdés 2: ha van eltérés a kapott eredmény és az elmélet között, az vajon a "cinkelés" miatt van vagy csak a véletlen hatások kusza összjátéka, mint a NORAD radarernyőin megcsillanó rádiójel a Vénuszról egy vadkacsa seggén interferálva, ahogyan éppen egy zuhanó orosz nukleáris töltetnek néz ki - és ezzel azonnali DEFCON 1-be állítja a Szabadság Földjét :DDD
Remélem elég színes választ adtam a kérdéseidre :)))
- A matricák számozottak 1-től 200-ig.
- Az albumban is számozott üres helyek vannak 1-től 200-ig.
- Mindenkit a saját helyére illik ragasztani, azaz a Mélytengeri baszikrája (Profundum mare piscii improvidii, L.) ne kerüljön a Pirosseggű makákó (Macacus rufus fundii, L.) helyére.
- Az albumban az összesen 200db matrica helyre már beragasztottunk 80db-ot és 120db van üresen.
- Kezünkbe nyomtak 185db totálisan random matricát.
- Elkezdjük ragasztani az üres 120db helyre azokat, amik még hiányoznak.
- Lesznek feleslegesek, lesznek, amik hiányoztak.
- Végigmentünk a 185db matricán, kérdés: hány olyan hely maradt az albumban, ahová nem ragasztottunk?
Mi megcsináltuk a ragasztást és megszámoltuk az üresen maradt helyeket és azt kaptuk, hogy negyvenkettő.
Kérdés 1: mennyi lenne ez a 42 elméletileg, amit a fentiek ismeretében várhattunk volna?
Kérdés 2: ha van eltérés a kapott eredmény és az elmélet között, az vajon a "cinkelés" miatt van vagy csak a véletlen hatások kusza összjátéka, mint a NORAD radarernyőin megcsillanó rádiójel a Vénuszról egy vadkacsa seggén interferálva, ahogyan éppen egy zuhanó orosz nukleáris töltetnek néz ki - és ezzel azonnali DEFCON 1-be állítja a Szabadság Földjét :DDD
Remélem elég színes választ adtam a kérdéseidre :)))
ZilogR
Nov 8, 2014, 6:35:59 AM11/8/14
to szamo...@googlegroups.com
Ennél puritánabb, hétköznapibb dolgot már nem tudok, mint a matrica ragasztás...
- Vagy legyen a klasszik példa a 15C kézikönyvből, kicsit átdolgozva a hétvégi piacolásra:
Balfékék elmennek a piacra. (direkt nem írtam Balf@szt, pedig sokkal jobban mutatna...)
Balfék Mama elkölt 1250Ft-ot és vásárol 4kg krumplit és répát (de szegény olyan hülye, hogy nem tudja, miből mennyit),
Balfék Papa is bevásárol, mert elfelejti, hogy neki nem kellett volna, ő is elkölt 1320Ft-ot és hazamegy 4kg krumplival és répával megintcsak vegyesen (mert ő is éppolyan hülye, mint a kedves neje).
Kérdés: ha a krumpli kilója 350Ft, a répáé 250Ft, akkor mennyit vásárolt ez a két szerencsétlen krumpliból és répából külön-külön?
Ez már olyan szinten volt primitív, hogy fájt... :DDD - Ha a Coca-Cola javarész foszforsavat tartalmaz, akkor mennyi a pH-ja, ha a foszforsav többértékű sav és több lépésben disszociál?
Elrohad-e ettől a fogunk?
És a gyomrunk?
És az agyunk...? - A szobában 70% relatív páratartalmat mérünk és a fal melletti levegőréteg hőátadási tényezője 8W/(m^2×K). A szobahőmérséklet 20C, kint pedig farkasordító -20C van. Vajon hány fokra kell csökkennie a belső hőmérsékletnek, hogy a falon megjelenjenek az első páracseppek és kezdetét vehesse a lakóparki zöld rohadás a falakon? A falat 30cm-es tégla + 5cm-es hungarocell-ként modellezzük.
- Egy TZ4K kistraktorral hajtott ágaprító vágókése 20cm átmérőjű körön jár körbe ~240fordulat/perc fordulatszámmal. Milyen magasra tudja dobni az aprítékot legfeljebb? Milyen fordulatszámon kell járatni, ha a vágókéstől 1.5m magasságig fel akarjuk dobni?
- ...más egyéb?
Ezek MIND hétköznapi példák, csak senki sem számol ilyeneket ki... :)
ZilogR
Nov 8, 2014, 10:59:47 AM11/8/14
to szamo...@googlegroups.com
Attila Válinth
Nov 13, 2014, 10:08:57 AM11/13/14
to szamo...@googlegroups.com
Megjósolja a jövőt egy számítógépes algoritmus a telefonos és közösségi oldalakon való tevékenység alapján. Kidolgozhatjuk a választ, mielőtt a kérdés befutna.... :) :)
Attila Válinth
Nov 14, 2014, 12:49:58 PM11/14/14
to szamo...@googlegroups.com
Sehunn senki...:)
ZilogR
Nov 15, 2014, 4:04:22 AM11/15/14
to szamo...@googlegroups.com
Dehogynem, csak az én akadémikus ötleteimre általában nincs reakció. Ha valami hadvezér lennék és kiállnék az amúgy harcra kész emberek elé és elmondanám, hogy akkor most menjünk csatázni és csináljuk ezt meg azt, mindenki hazamenne, hogy "jó, hát végülis, igen, csatázni akarnánk, de igazából már nincs is hozzá kedvünk, ha ez ilyen macerás, meg amúgy is a fémes csengése a kardoknak, meg az az ágyúropogás" :DDD ;) ;)
Attila Válinth
Nov 15, 2014, 2:22:19 PM11/15/14
to szamo...@googlegroups.com
Jó vezér vagy te...:)
ZilogR
Nov 16, 2014, 9:34:54 AM11/16/14
to szamo...@googlegroups.com
"Csak egy vezér van: Rákóczi" "Rákóczi? Egy túróst..."
Ext! Ha már a 15C-vel nem akarsz ;) okosságokat programozni, akkor - mert te bele vagy szerelmesedve a 4500P-dbe - arra írj valami okosságot! Az azért elég jó kis gépecske. Pl.: kipróbálhatod a sűrűségfüggvényes feladványt - de ahhoz kell írnod egy solve rutint. Arra jó lehet egy egyszerű szelő módszer, a gép meg tud integrálni. Az Euler-t is megírhatod, annyira egyszerű, hogy szégyenkezni fogsz, hogy erre a pofonegyszerű feladatra időt pazaroltál...
Ext! Ha már a 15C-vel nem akarsz ;) okosságokat programozni, akkor - mert te bele vagy szerelmesedve a 4500P-dbe - arra írj valami okosságot! Az azért elég jó kis gépecske. Pl.: kipróbálhatod a sűrűségfüggvényes feladványt - de ahhoz kell írnod egy solve rutint. Arra jó lehet egy egyszerű szelő módszer, a gép meg tud integrálni. Az Euler-t is megírhatod, annyira egyszerű, hogy szégyenkezni fogsz, hogy erre a pofonegyszerű feladatra időt pazaroltál...
Attila Válinth
Nov 17, 2014, 11:39:42 AM11/17/14
to szamo...@googlegroups.com
Jó az a kis HP15 is.
Valami kérdést kiagyalok, hogy agyalhassunk..:)
ZilogR
Dec 6, 2014, 1:00:09 PM12/6/14
to szamo...@googlegroups.com
Azóta leesett-é a tantusz Ext barátom?!?! :)))
Tessék megnézni, hogy mit csinál ez a 7+5 utasítás és megérteni, mert ez egy nagyon jó kis példa arra, amit amúgy te kértél - és nem is bonyolult!!! :) ;)
Tessék megnézni, hogy mit csinál ez a 7+5 utasítás és megérteni, mert ez egy nagyon jó kis példa arra, amit amúgy te kértél - és nem is bonyolult!!! :) ;)
Attila Válinth
Dec 14, 2014, 12:49:05 PM12/14/14
to szamo...@googlegroups.com
Halllooooooooooooooooooooooooooo :D
ZilogR
Dec 14, 2014, 2:39:46 PM12/14/14
to szamo...@googlegroups.com
Akkor megvan a megoldás?!? Ez azt jelenti, vagy nem?!??!
ZilogR
Dec 15, 2014, 2:15:07 AM12/15/14
to szamo...@googlegroups.com
Pedig azt hittem, hogy beindul a dolog, anno a világvége topik is december 14-én indult. Lehet az utolsó napokra gyűjteni a municiót, hogy legyen két hét pörgés az év végén.
ZilogR
Dec 25, 2014, 12:55:38 PM12/25/14
to szamo...@googlegroups.com
És vat iz dö szityuésön?!
Attila Válinth
Dec 28, 2014, 7:03:38 AM12/28/14
to szamo...@googlegroups.com
Sziasztok!
Na mi történt itt? :)
2014. december 25., csütörtök 18:55:38 UTC+1 időpontban ZilogR a következőt írta:
2014. december 25., csütörtök 18:55:38 UTC+1 időpontban ZilogR a következőt írta:
És vat iz dö szityuésön?!
ZilogR
Dec 28, 2014, 9:03:29 AM12/28/14
to szamo...@googlegroups.com
Az a gond, hogy semmi... :)
Az indító postok körül volt egy olyan, hogy engem nagyon érdekelnek a robbanások, lökéshullámok - levegőben vagy talajban - és belefutottam a Trinity Test-tel kapcsolatban Fermi becslésébe (Link) Vajon milyen módszert használhatott a becsléshez?!? (Én egyszerű középsulis fizikával 138kT-t becsültem, de a modell nem túl jó.)
Az indító postok körül volt egy olyan, hogy engem nagyon érdekelnek a robbanások, lökéshullámok - levegőben vagy talajban - és belefutottam a Trinity Test-tel kapcsolatban Fermi becslésébe (Link) Vajon milyen módszert használhatott a becsléshez?!? (Én egyszerű középsulis fizikával 138kT-t becsültem, de a modell nem túl jó.)
ZilogR
Dec 31, 2014, 8:05:04 PM12/31/14
to szamo...@googlegroups.com
Háát, ezt nem gondoltam volna, de ennek köszönhetően én lettem a kis monológjaimmal a legtöbbet postoló decemberben (asszem). :D
Sztem megtartom magamnak a sziporkáimat és jelentkezem, ha alkottam valamit ;)
Mindenesetre ne határolódjatok el a hozzászólásoktól!
BUÉK mindenkinek és várom a postokat!
Sztem megtartom magamnak a sziporkáimat és jelentkezem, ha alkottam valamit ;)
Mindenesetre ne határolódjatok el a hozzászólásoktól!
BUÉK mindenkinek és várom a postokat!
Attila Válinth
Jan 2, 2015, 1:04:06 PM1/2/15
to szamo...@googlegroups.com
BUÉK!
α = 137,5 ̊ ... :)
Mengyán Zsolt
May 11, 2015, 5:04:48 PM5/11/15
to szamo...@googlegroups.com
Sziasztok!
A minap a kezembe nyomtak egy TI-92+-t (tulajdonjogilag még nem enyém, de ami késik, nem múlik :-) ), és a neten rákeresve ide jutottam. A topik láttán felcsillant a szemem, mert van egy probléma, ami régóta foglalkoztat, itt meg hétköznapi életben adódó bonyolult feladatok után sóhajtoznak :-). Íme! Adott egy fekvő hengeres tartály. Átmérője 2 méter, hossza 3 méter. A két végén gömbszelettel van lezárva, amelynek magassága 0,2m. Van a tartályban 60cm folyadék (pl benzin). Hány liter van benne? Mivel már nem "három-hatvan" a benzin (de lesz még, csak euro-ban), és a tartály tartalma raktárkészletnek minősül, így a lehető legpontosabb meghatározásra van szükség, amihez viszont mindenképpen figyelembe kell venni a véglezáró gömbszeleteket.
A minap a kezembe nyomtak egy TI-92+-t (tulajdonjogilag még nem enyém, de ami késik, nem múlik :-) ), és a neten rákeresve ide jutottam. A topik láttán felcsillant a szemem, mert van egy probléma, ami régóta foglalkoztat, itt meg hétköznapi életben adódó bonyolult feladatok után sóhajtoznak :-). Íme! Adott egy fekvő hengeres tartály. Átmérője 2 méter, hossza 3 méter. A két végén gömbszelettel van lezárva, amelynek magassága 0,2m. Van a tartályban 60cm folyadék (pl benzin). Hány liter van benne? Mivel már nem "három-hatvan" a benzin (de lesz még, csak euro-ban), és a tartály tartalma raktárkészletnek minősül, így a lehető legpontosabb meghatározásra van szükség, amihez viszont mindenképpen figyelembe kell venni a véglezáró gömbszeleteket.
ZilogR
May 12, 2015, 3:29:08 AM5/12/15
to szamo...@googlegroups.com
:) a(!) klasszikus kalkulátor feladat. Én még ráadásként vegyipari gépész is vagyok, akár szerethetném is ezt a feladatot, de bevallom, már kiskorom óta utálom.
Annak idején általános iskolában a sulinak nem volt pénze HT1080Z, Spectrum, Commodore számítókat venni de a számítástechnika fakultációt - Isten áldja a tanárnőt, hálás vagyok neki ezért nagyon - 6db Texas Instruments TI-57LCD típusú számológéppel elindították. Akkor voltam negyedik osztályos, azaz éppen 10 éves. Olyan korban, amikor egy kis vidéki iskola csak álmodhatott számítógépekről, mi már mindent tudtunk a programozásról és külön jutalom volt egy hétvégére elvinni egy-egy számológépet. Több tucat apró kis algoritmuson keresztül tanultunk meg programozni.
Annak a korszaknak vannak a témába vágó könyvei és ezek klasszikus példája, amit te itt leírtál - na, ez volt az a példa, amit soha, de soha nem oldottam meg - és később sem, nagyobb fejjel, komolyabb eszközökkel sem.
Így hát, rátok hárul ez a szépnek nem nevezhető favágó feladat :)
Sok sikert! :D
Annak idején általános iskolában a sulinak nem volt pénze HT1080Z, Spectrum, Commodore számítókat venni de a számítástechnika fakultációt - Isten áldja a tanárnőt, hálás vagyok neki ezért nagyon - 6db Texas Instruments TI-57LCD típusú számológéppel elindították. Akkor voltam negyedik osztályos, azaz éppen 10 éves. Olyan korban, amikor egy kis vidéki iskola csak álmodhatott számítógépekről, mi már mindent tudtunk a programozásról és külön jutalom volt egy hétvégére elvinni egy-egy számológépet. Több tucat apró kis algoritmuson keresztül tanultunk meg programozni.
Annak a korszaknak vannak a témába vágó könyvei és ezek klasszikus példája, amit te itt leírtál - na, ez volt az a példa, amit soha, de soha nem oldottam meg - és később sem, nagyobb fejjel, komolyabb eszközökkel sem.
Így hát, rátok hárul ez a szépnek nem nevezhető favágó feladat :)
Sok sikert! :D
Attila Válinth
May 16, 2015, 2:25:44 PM5/16/15
to szamo...@googlegroups.com
Okos kis feladat :)
2015. május 11., hétfő 23:04:48 UTC+2 időpontban Mengyán Zsolt a következőt írta:
ZilogR
May 17, 2015, 7:47:02 AM5/17/15
to szamo...@googlegroups.com
:) igazából ebben ott van a probléma, hogy 60cm benne a folyadékszint. Mert ha ez egy valós feladat, akkor azt hogyan és milyen pontossággal méred - a fene egye meg, még a végén megcsinálom...
Attila Válinth
May 17, 2015, 8:19:31 AM5/17/15
to szamo...@googlegroups.com
gömbszelet térfogat!+henger térfogat
ha tele...
Így esetleg illeszkedő fv. (a gömbszeletre) térben integrálva 0-0,6 intervallumon...:) talán/vagy
Tolosa
May 17, 2015, 12:34:37 PM5/17/15
to szamo...@googlegroups.com
A 60 cm-es magasság problémára még találtam megoldást, nekem inkább a két gömbszelet lezárás okoz problémát.
Hengeres tartályban lévő folyadék mennyisége.
Hengeres tartályban lévő folyadék mennyisége.
2015. május 17., vasárnap 13:47:02 UTC+2 időpontban ZilogR a következőt írta:
Tolosa
May 17, 2015, 12:37:22 PM5/17/15
to szamo...@googlegroups.com
Mondjuk, EZEN az oldalon van némi segítség arra a problémára is, de ezt még át kell nyálazni.
gyapo
May 17, 2015, 1:25:20 PM5/17/15
to szamo...@googlegroups.com
Tolosa, you wrote:
T> Mondjuk, EZEN
T> <http://matematikasegito.blogspot.hu/2013/03/a-gomb-felszine-es-terfogata.html>az
T> oldalon van némi segítség arra a problémára is, de ezt még át kell nyálazni.
Gömbszelet térfogata a függvénytáblázatból:
(pi/3)*m^2*(3R-m)
ahol R a gömb sugara, r a szelet metszési kerületének körének sugara,
m a szelet magassága. A fele magasságnál fél térfogat lesz, de hogy a
szint változásával milyen módon változik, azt nem tudom. Szögfüggvény
módosítva az R/r aránnyal?
Üdv.: gyapo
T> Mondjuk, EZEN
T> <http://matematikasegito.blogspot.hu/2013/03/a-gomb-felszine-es-terfogata.html>az
T> oldalon van némi segítség arra a problémára is, de ezt még át kell nyálazni.
Gömbszelet térfogata a függvénytáblázatból:
(pi/3)*m^2*(3R-m)
ahol R a gömb sugara, r a szelet metszési kerületének körének sugara,
m a szelet magassága. A fele magasságnál fél térfogat lesz, de hogy a
szint változásával milyen módon változik, azt nem tudom. Szögfüggvény
módosítva az R/r aránnyal?
Üdv.: gyapo
Pipás
May 18, 2015, 4:01:39 AM5/18/15
to szamo...@googlegroups.com
Ez biztos valami olyasmi lesz hogy a gömbszeletet vízszintesen fel kell szelni sok apró hasábra és ezek térfogtát összeadogatni. A hasábok hossza a henger körének egyenlete szerint fog változni. A hasábok alapjának vízszintes mérete meg a gömbszelet körének egyenlete szerint. Ehhez ki kell számolni a gömbszelet gömbjének a sugarát...
?
?
Attila Válinth
May 19, 2015, 12:03:08 PM5/19/15
to szamo...@googlegroups.com
Igen. nem is könnyű annyira...
Pipás
May 20, 2015, 2:41:46 AM5/20/15
to szamo...@googlegroups.com
Találtam egy gyakorlati módszert, ami persze nem az igazi megoldás.
https://www.google.hu/url?sa=t&source=web&rct=j&ei=bhpcVcHuAoTxUq3hgdAB&url=http://mkeh.gov.hu/index.php%3Fname%3DOE-eLibrary%26file%3Ddownload%26keret%3DN%26showheader%3DN%26id%3D9631&ved=0CCcQFjAC&usg=AFQjCNH0h7JIqfNaOjhl7PWGBYYXXLKO9g&sig2=VJcOL-ulv9EJj7Hn1WLRlg
Ez gondolom a mérésügyi hivatal pdf-je. A 2 legfontosabb oldalt külön mellékeltem. Ki tudjuk számolni a hengeres rész és a gömbsüvegek össztérfogatát. Adott h töltési magassághoz kiszámoljuk a töltési magasság és a henger sugarának hányadosát (h/r). Ezzel a táblázatból kapunk 2 korrekciós tényezőt amivel kiszámolható a töltési magassághoz tartozó térfogat. Az lenne az igazi ha mi magunk tudnánk a gömbsüvegek résztérfogatát koszámolni...
https://www.google.hu/url?sa=t&source=web&rct=j&ei=bhpcVcHuAoTxUq3hgdAB&url=http://mkeh.gov.hu/index.php%3Fname%3DOE-eLibrary%26file%3Ddownload%26keret%3DN%26showheader%3DN%26id%3D9631&ved=0CCcQFjAC&usg=AFQjCNH0h7JIqfNaOjhl7PWGBYYXXLKO9g&sig2=VJcOL-ulv9EJj7Hn1WLRlg
Ez gondolom a mérésügyi hivatal pdf-je. A 2 legfontosabb oldalt külön mellékeltem. Ki tudjuk számolni a hengeres rész és a gömbsüvegek össztérfogatát. Adott h töltési magassághoz kiszámoljuk a töltési magasság és a henger sugarának hányadosát (h/r). Ezzel a táblázatból kapunk 2 korrekciós tényezőt amivel kiszámolható a töltési magassághoz tartozó térfogat. Az lenne az igazi ha mi magunk tudnánk a gömbsüvegek résztérfogatát koszámolni...
Pipás
May 20, 2015, 2:49:43 AM5/20/15
to szamo...@googlegroups.com
Edit: kiszámolni...
(Retkes tablet... :( )
(Retkes tablet... :( )
Message has been deleted
Tolosa
May 20, 2015, 6:14:08 AM5/20/15
to szamo...@googlegroups.com
Ne keseredj el, a 'szarókázás' is így született!:-)
Message has been deleted
Pipás
May 20, 2015, 7:52:02 AM5/20/15
to szamo...@googlegroups.com
Szintén tableten?
Tolosa
May 20, 2015, 8:54:17 AM5/20/15
to szamo...@googlegroups.com
Mármint most? Nem. sajnos a tabletemet elkommunizálta a Zasszony!:-)
Szóval az előbb azt akartam mondani, hogy ezt a gömbsüveg-problémát valószínűleg integrál számítással tudjuk megoldani, csak jobban bele kéne mélyedni.
2015. május 20., szerda 13:52:02 UTC+2 időpontban Pipás a következőt írta:
Szóval az előbb azt akartam mondani, hogy ezt a gömbsüveg-problémát valószínűleg integrál számítással tudjuk megoldani, csak jobban bele kéne mélyedni.
2015. május 20., szerda 13:52:02 UTC+2 időpontban Pipás a következőt írta:
Szintén tableten?
Pipás
May 20, 2015, 10:44:39 AM5/20/15
to szamo...@googlegroups.com
Ja. :)
ZilogR
May 21, 2015, 12:37:16 AM5/21/15
to szamo...@googlegroups.com
Várjatok még egy kicsit, megint üzembehelyezek és ma este utazok el az erőműből, holnap hazarepülök és a tiétek vagyok :-)
Tolosa
May 21, 2015, 3:42:16 AM5/21/15
to szamo...@googlegroups.com
Tudom, hogy ez nem megoldás a megoldásra, de szarókázásilag megtekinthető: egy konkrét, grafikával illusztrált eredmény a konkrét feladatra /is/. Persze az üzemanyag mennyiség meghatározása itt is a két gömbsüveg nélkül történik.:-(
ITT.
2015. május 20., szerda 16:44:39 UTC+2 időpontban Pipás a következőt írta:
ITT.
2015. május 20., szerda 16:44:39 UTC+2 időpontban Pipás a következőt írta:
Ja. :)
It is loading more messages.
0 new messages